수술불가 1~2차 항암 치료에 면역·표적항암제 보험급여 전무
예후가 불량한 대표적인 암종인 담도암의 치료가 빠르게 변하고 있다. 면역 및 표적 항암제들이 봇물 터지듯 개발돼 나온 것. 하지만 국내에선 보험급여가 적용되는 약이 전무해 여전히 '신약 불모지'와 다름없다는 비판이 일고 있다.
2023년에 발표된 중앙암등록본부 자료에 따르면, 한국에서 담도암은 전체 암 발생의 2.7%로 9위를 차지하고 있는 암종이다.
발생 빈도는 낮지만 조기 진단이 어렵고, 주변 장기나 림프절로 전이가 잘 돼 평균적으로 예후가 좋지 않은 암종으로 알려져 있으며, 국내에서 5년 상대생존율(2017~2021년)은 남녀 전체 28.9%로 보고됐다. 원격 전이가 있는 환자의 경우에는 5년 상대생존율이 3.2%로 현격하게 떨어지는 무서운 암종이다.
하지만 최근 이런 담도암에 괄목할 만한 발전이 있었다. 근치적 절제가 불가한 국소 진행성, 진행성 혹은 전이성 환자의 항암치료에 면역항암제 및 표적항암제들이 속속 개발되며 과거와는 다르게 정밀의료가 가능한 분야로 거듭나고 있기 때문.
과거에는 '젬시타빈/시스플라틴(이하 'GemCis')', 'FOLFOX' 등 화학요법이 1~2차 치료에 주를 이뤘다면, 이젠 1차 치료에 항 PD-(L)1 면역항암제 병용, 2차 치료에 IDH1·FGFR2·BRAF·HER2 억제제 등을 활용한 유전자 변이에 따른 표적치료가 표준요법으로 자리 잡았다.
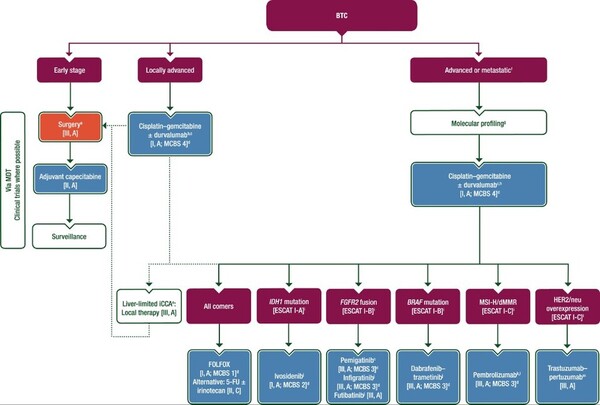
실제 유럽종양학회(ESMO) 가이드라인에서는 국소 진행성, 진행성 혹은 전이성 담도암으로 진단된 환자에서 1차 치료에 '더발루맙(제품명 임핀지) + GemCis' 병용을 표준치료로 권고하고 있으며, 이후 질병이 진행된 2차 치료엔 유전자 변이에 따른 각각의 표적항암제 및 면역항암제 등을 권고하고 있다(그림).
IDH1 변이가 있다면 '이보시데닙' 단독요법, FGFR2 융합이 있다면 '페미가티닙(제품명 페마자이레)' 혹은 '푸티바티닙' 단독요법, BRAF 변이가 있다면 '다브라페닙(제품명 라핀나) + 트라메티닙(제품명 매큐셀)' 병용요법, MSI-H/dMMR 환자라면 '펨브롤리주맙(제품명 키트루다)' 단독요법, HER2/nue 과발현 환자라면 '트라스트주맙 + 퍼투주맙(제품명 퍼제타)' 병용요법이 권고된다.
하지만 위에 언급된 신약들 중 국내에서 급여로 쓸 수 있는 약은 전무하다. 아직 국내 도입되지 않은 '이보시데닙'과 '푸티바티닙'은 차치하더라도, 이미 도입돼 다른 암종에서 사용되고 있는 약제들 역시 모두 급여도 적용되지 않고 사전신청을 통해 사용할 수밖에 없어 접근성이 현저히 떨어져 있다.
작년 한독이 '페마자이레' 허가와 동시에 보험급여를 신청했지만 건강보험심사평가원 암질환심의위원회(이하 암질심)에서 재심의 끝에 급여기준 설정에 실패했다. 아스트라제네카는 2022년 말 '임핀지 + GemCis' 병용요법을 허가 받고 이듬해 급여를 신청했지만 이 역시 암질심 단계에서 좌초됐다.
그나마 다행인 점은 과거에는 환자들이 자비로 '임핀지'를 사용하고자 할 경우 함께 병용하는 'GemCis'마저 비급여로 전화돼 환자들의 부담이 가중되는 문제가 있었지만, 작년 11월 암질심에서 임핀지와 병용하는 GemCis 요법에 대해서는 '본인일부부담(5/100)'으로 인정해 임핀지만 100% 본인부담으로 사용할 수 있게 됐다는 것이다.
이밖에 한국MSD는 작년 '치료 이력이 있고 대체 치료 옵션이 없는 MSI-H/dMMR인 전이성 고형암' 등을 포함한 키트루다의 13개 적응증을 일괄 급여 신청해 현재 암질심으로부터 심사를 받고 있지만, 담도암은 여기에 포함되지 않았다.
이처럼 '허가사항에 없어서', '급여가 안 돼서', '약값이 비싸서' 등의 이유로 눈 앞에 치료제를 두고도 쓸 수 없는 국내 담도암 환자들은 최적의 치료로부터 한발 더 멀어지고 있는 현실이다.
〈코리아헬스로그 자매지 '청년의사'에 게재된 기사입니다.〉
